3º) Trabalho de um
Processo Cíclico


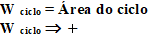
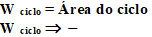
3.5 Trabalho do Não-Equilíbrio

Supondo que a membrana da figura rompa-se,
permitindo que o gás expanda-se e preencha o
volume com vácuo. Não há resistência a expansão
do gás no contorno em movimento conforme ele
preenche o volume. Portanto não há trabalho
realizado, ainda que haja mudança no volume.
Trabalho de um Gás Perfeito
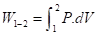 ou
ou
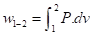
A) Processos
Politrópicos
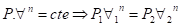
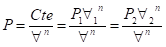

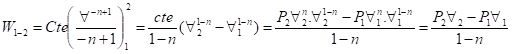

OBS: Não é válido
para n = 1 (isotérmica)
B) Processo Isobárico
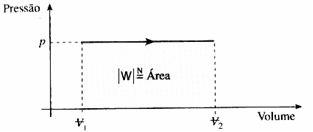
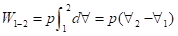
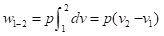
C) Processo Isométrico
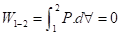
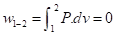
D) Processo Isotérmico
ou
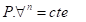 ®
Processo politrópico
®
Processo politrópico
Isotérmica
Þ n =
1
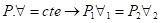

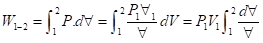
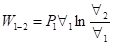
exercícios - Lista 3
1. Considere como um sistema
o gás contido no cilindro mostrado na figura; o
cilindro é dotado de um pistão sobre o qual
foram colocados vários pequenos pesos. A pressão
inicial é de 200 kPa e o volume inicial do gás é
de 0,04 m3.
A) Um bico de Bunsen aceso
é colocado embaixo do cilindro até que o volume
do gás aumente para 0,1 m3, enquanto a pressão
permanece constante. Calcule o trabalho
realizado pelo sistema durante esse
processo.(12,0 kJ)
B) Considere o mesmo
sistema e as mesmas condições iniciais, porém,
ao mesmo tempo em que o bico de Bunsen está sob
o cilindro e o êmbolo se levanta, os pesos são
removidos de maneira que a temperatura do gás
permanece constante durante o processo. (7,3 kJ)
C) Considere o mesmo
sistema; porém, durante a transferência de
calor, os pesos são removidos de maneira que a
expressão P V1,3 = constante descreve a
relação entre a pressão e o volume durante o
processo. Novamente, o volume final é 0,1 m3.
Calcule o trabalho. (6,41kJ)
D) Considere o sistema e os
estados inicial dados nos três primeiros itens,
porém com o êmbolo retido por um pino de modo
que o volume permaneça constante. Além disso, o
calor é transferido do sistema até que a pressão
caia para 100 kPa. Calcule o trabalho. (Zero)
2. A um aparato de pistão e
cilindro, adiciona-se energia. O pistão é puxado
de tal maneira que a
quantidade pV =
constante. A pressão e o volume iniciais são 200
kPa e 2 m3, respectivamente. Se a pressão final
é 100 kPa, calcule o trabalho realizado pelo gás
no pistão. (277 kJ)
3. Ar expande-se em um
aparato de pistão e cilindro a uma pressão
constante de 200 kPa, passando de um volume de
0,1 m3 para um volume de 0,3 m3. Em seguida, a
temperatura é mantida constante durante uma
expansão de 0,5 m3. Determine o trabalho total
realizado pelo ar. (98,8 kJ)
4. Se 10 kg de ar
(comportando-se como um gás ideal), inicialmente
à pressão de 1,7 x 106 N/m2 sofrem um decréscimo
de volume de 1,8 m3 para 0,6 m3, permanecendo a
pressão constante, qual é o trabalho executado?
É positivo ou negativo? (-2,04x10+6 J)
5. Se 3kg de ar sofrem um
processo isotérmico quase estático, qual é a
pressão final, se a pressão e o volume iniciais
são, respectivamente, 5,16 x105 N/m2 e 0,3 m3, e
executa-se um trabalho de 3,12 x 10 4 J sobre o
ar (considere o ar um gás ideal)? (6,3.105 Pa)
6. Qual o conceito
termodinâmico de trabalho?
7. O que significa dizer
que o trabalho não é uma propriedade de estado?
8. O que representa um
diferencial inexato?
9. 12 g de um gás ocupam o
volume de 5.10-3 m3 a temperatura de – 3ºC. O
gás é aquecido à pressão constante até sua massa
específica tornar-se igual a 2.10-3 g/cm3.
Calcule a temperatura neste estado. (51ºC)
10. Calcule o número de
moles de 2 kg de cada uma das seguintes
substâncias: CH4 (metano), C2 H4 (acetileno).
(125 mols, 71,43 mols)
11. Um gás monoatômico em
um recipiente ocupa 0,042 m3 a 27ºC e 15.106 Pa.
Calcule:
a) o número de moles
contido no tanque. (252,71 mols)
b) O volume específico
molar. (1,66.10-4 m3/mol)
12. Um tanque de 0,42m3 de
volume contém oxigênio à pressão de 1,5.107 N/m2
e à temperatura de 21ºC. Suponha que o oxigênio
se comporte como um gás ideal. Dado: ROxigênio =
0,2598 kJ/kgK
a) Quantos quilomols contêm
o tanque? (2,577 kmol)
b) Quantos quilogramas?
(82,48 kg)
c) Qual a pressão quando a
temperatura eleva-se a 980ºC? (6,39.107 Pa)
d) Quantos kg podem ser
retirados do tanque, à temperatura de 21ºC,
antes que a pressão caia até 1,5.105N/m2?
(8,1655.103 kg)
13. Um sistema que consiste
em 2kg de um gás é submetido a um processo
durante o qual a relação entre pressão e o
volume específico é pv1/3 = constante. O
processo se inicia com pressão de 105 Pa, volume
específico de 0,5 m3/kg e finda com pressão de
0,25.105 Pa. Determine o volume final e
represente o processo em um gráfico p x v. (64
m3)
14. 2 kg de ar sofrem um
processo isotérmico quase-estático, qual é a
pressão final, se a pressão e o volume iniciais
são, respectivamente, 4,0.105 Pa e 0,2 m3, e
neste processo o gás executa um trabalho de
3,2.104J? (2,68.105 Pa)
15. 1,5 kg de neônio,
considerado gás perfeito, a pressão atmosférica
e 100ºC sofre um processo isovolumétrico quase
estático até reduzir a pressão a metade; logo
após sofre um processo isotérmico quase estático
até dobrar o volume. Calcule: Dado: cp = 1,020
kJ/kgK e cv = 0,618 kJ/kgK
a) o trabalho total; (80,56
kJ)
b) o calor total. (-92,29
kJ)
16. Quando um sistema não
troca calor com o meio, sua temperatura
obrigatoriamente permanece constante. Comente a
afirmativa.
Clique aqui
para acessar a resolução dos exercícios